Bei diesem Andocken an die Zelle klappt das Glykoprotein B auf und bildet Fortsätze, die in die Zellmembran eindringen. Dies leitet die Verschmelzung der Virenhülle mit der Membran ein und öffnet dem Virus den Weg in die Zelle. Könnte man dieses Glykoprotein blockieren, ließe sich die Infektion der Zelle verhindern – womöglich nicht nur bei Herpes simplex, sondern auch anderen Herpesviren. Bisher scheiterten jedoch alle Versuche, solche Antikörper zu entwickeln, wie Vollmer und seine Kollegen berichten.
Das Problem: Entscheidende Ansatzstellen des Glykoprotein B sind vor der Infektion in einer tiefen Falte verborgen und nahezu unzugänglich. Dadurch hat das Immunsystem keine Chance, passende Antikörper gegen dieses virale Protein zu bilden. Diese wären außerdem zu groß, um in die Falte zu passen. Hinzu kommt eine raffinierte Ablenkungsstrategie der Herpesviren: Sie präsentieren der Immunabwehr andere, exponiert platzierte Glykoproteine als Erkennungsmerkmale und Angriffsziel. Lagern sich Antikörper daran an, schadet dies dem Virus aber nicht.
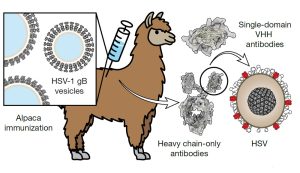 Die modifizierten Herpes-Glykoproteine wurden auf synthetische Vesikel appliziert und dem Alpaka injiziert. Dieses produzierte daraufhin Mini-Antikörper, deren neutralisierende Wirkung auf Herpes simplex (HSV) in Zellversuchen getestet wurde. © Vollmer et al./ Nature, /CC-by 4.0
Die modifizierten Herpes-Glykoproteine wurden auf synthetische Vesikel appliziert und dem Alpaka injiziert. Dieses produzierte daraufhin Mini-Antikörper, deren neutralisierende Wirkung auf Herpes simplex (HSV) in Zellversuchen getestet wurde. © Vollmer et al./ Nature, /CC-by 4.0
Mini-Antikörper vom Alpaka
Vollmer und seinem Team ist es nun erstmals gelungen, die genaue Struktur der verborgenen Ansatzstellen mittels Kryoelektronenmikroskopie zu entschlüsseln. Dies ermöglichte es ihnen, durch eingefügte Mutationen eine aufgeklappte Version dieses viralen Glykoproteins zu erzeugen. Die entscheidenden Ansatzstellen lagen dadurch offen. Dieses veränderte Virusprotein injizierten die Forschenden anschließend einem Alpaka. Diese Kamelverwandten sind dafür bekannt, besonders kleine, einfache Antikörper zu produzieren.
Das mit dem modifizierten Herpesvirus-Protein „geimpfte“ Alpaka erzeugte mehrere unterschiedliche Antikörper gegen das Glykoprotein B. Diese Mini-Antikörper reduzierten Vollmer und sein Team dann im nächsten Schritt auf die entscheidende Andockstelle – den Schlüssel für das „Schloss“ des viralen Glykoproteins. Dadurch entstanden winzige Nanobodies, die in Hefezellen gezüchtet und vermehrt werden konnten. Diese Nanobodies haben die Forschenden dann in Zellkulturen auf ihre Wirkung gegen Herpes simplex 1 und 2 getestet.
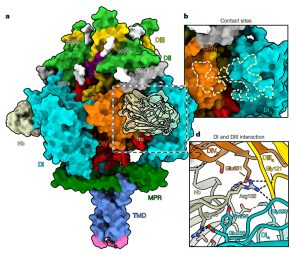 Struktur des Glykoprotein B eines Herpesvirus mit angedocktem Nanobody. © Vollmer et al./ Nature, /CC-by 4.0
Struktur des Glykoprotein B eines Herpesvirus mit angedocktem Nanobody. © Vollmer et al./ Nature, /CC-by 4.0
Nanobody neutralisiert beide Herpes-simplex-Varianten
Das Ergebnis: „Wir konnten dabei genau einen Nanobody identifizieren, der eine starke neutralisierende Wirkung hat“, berichtet Seniorautor Dirk Görlich vom Max-Planck-Institut für Multidisziplinäre Naturwissenschaften on Göttingen. Der Mini-Antikörper Nb1_gbHSV neutralisierte schon bei einer Konzentration von 1,2 Nanomol die Hälfte aller Viren. „Spannend ist, dass er sowohl gegen HSV 1 als auch HSV-2 wirkt“, sagt Görlich.
Nähere Analysen ergaben, dass der Nanobody sich so an der Ansatzstelle des Glykoproteins anlagert, dass dieses nicht mehr aufklappen kann. „Unsere Ergebnisse legen nahe, dass die Bindung des Nanobodies das Protein daran hindert, seine Form so zu verändern, dass es die Membranen fusionieren kann“, erklärt Co-Seniorautor Kay Grünewald von der Universität Hamburg. „So wird die Infektion verhindert.“
Neue Chance gegen latente Herpesinfektionen
Damit eröffnen diese neuen Mini-Antikörper neue Chancen, Herpesinfektionen zu behandeln und ihnen vorzubeugen. Denn die Nanobodies wirken schon, bevor die Viren die Zellen infiziert und einen neuen Herpesausbruch eingeleitet haben. „Sie könnten zukünftig besonders gefährdete Personen vor einer Herpesinfektion oder dem erneuten Ausbrechen einer latenten Infektion schützen“, sagt Vollmer. Denkbar wäre es zum Beispiel, schwangere Frauen damit zu behandeln, um eine Ansteckung des Neugeborenen zu verhindern.
Bis es jedoch soweit ist, müssen erst noch weitere Tests folgen. In ihnen muss unter anderem geprüft werden, ob die Mini-Antikörper auch im lebenden Organismus gegen die Herpesviren wirken und ob ihr Einsatz unbedenklich ist. „Noch ist es ein längerer Weg, aber Menschen, deren Immunsystem besonders schwach ist, werden umso mehr von den innovativen Antikörpern profitieren können“, sagt Vollmer. Er und sein Team haben bereits einen Patentantrag für den Nanobody eingereicht. (Nature, 2025; doi: 10.1038/s41586-025-09438-5)
Quelle: Nature, Universität Hamburg
5. September 2025
– Nadja Podbregar