Redacción
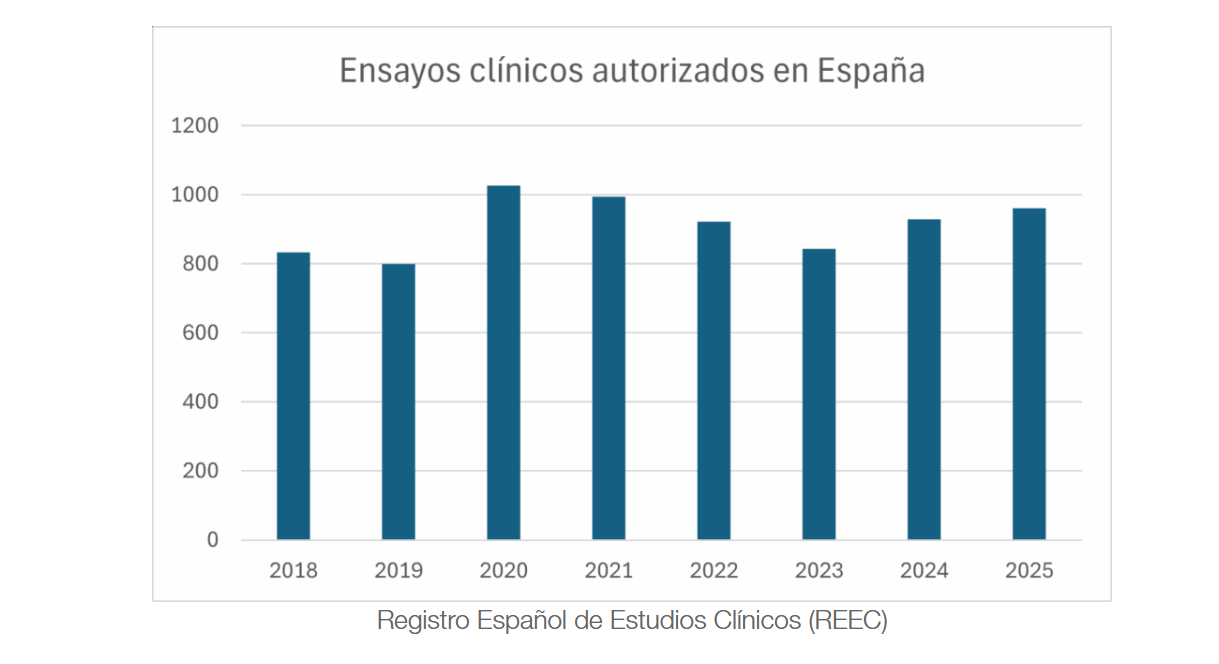
España volvió a situarse en 2025 como líder europeo en ensayos clínicos con medicamentos, tras autorizar 962 estudios, una cifra récord que consolida una década de crecimiento sostenido en investigación clínica. Los datos proceden del Registro Español de Estudios Clínicos (Reec), coordinado por la Agencia Española de Medicamentos y Productos Sanitarios (Aemps).
Este volumen sitúa a España no solo como el país con mayor número de ensayos autorizados, sino también como el que presenta mayor diversidad de áreas terapéuticas, en una fase clave del desarrollo de nuevos medicamentos que se extiende desde la investigación preclínica hasta su llegada a los pacientes.
El crecimiento, sostenido desde 2016, se ha intensificado especialmente en los dos últimos años, con más de un centenar de estudios adicionales respecto a ejercicios anteriores. Además, España se mantiene como el país europeo más activo en investigación clínica. Según los datos del Clinical Trials Information System (Ctis), en 2025 inició 849 ensayos clínicos, muy por delante de Francia (732), Alemania (711) e Italia (593).
España es con diferencia el país de Europa que más estudios inició en 2025 (849), seguido de Francia (732), Alemania (711) e Italia (593)
La oncología concentra cuatro de cada diez ensayos
La búsqueda de nuevos tratamientos contra el cáncer concentró el 40% de los ensayos clínicos, convirtiéndose en el área terapéutica con mayor número de estudios. España lidera también este ámbito en Europa, con hospitales de referencia a nivel continental. Tal y como destaca la Aemps, estos ensayos multicéntricos permiten reclutar suficientes pacientes en distintos países, obtener resultados robustos y acelerar el desarrollo de nuevos tratamientos.
Tras la oncología, las áreas con mayor actividad fueron las enfermedades del sistema inmunitario (10,5%), sistema nervioso (6,9%), cardiovasculares (6,2%) y respiratorias (4,4%). Además, el 22,5% de los ensayos se dirigieron a enfermedades raras, un ámbito prioritario de innovación.
En cuanto a las fases de desarrollo, los ensayos en fase I representaron el 25% y los de fase II el 31%, ambas en claro crecimiento. Estos datos reflejan, según la Aemps, la fortaleza del sistema español de investigación clínica, el alto nivel científico de los profesionales sanitarios y la posibilidad de ofrecer opciones terapéuticas más tempranas a los pacientes.
Juan Yermo: «Los cambios geopolíticos están transformando el panorama mundial de innovación en salud y es necesario actuar con urgencia para no perder la carrera global por la innovación»
Colaboración público-privada y reto geopolítico
El liderazgo español se apoya en varios factores clave: una red hospitalaria altamente capacitada, con cerca de 1.000 centros implicados en investigación clínica en los últimos cinco años; una elevada participación de pacientes, con tasas de reclutamiento entre las mejores de Europa; y una intensa colaboración público-privada. No en vano, más del 80% de los ensayos clínicos están financiados por la industria farmacéutica.
Este impulso resulta determinante en un contexto internacional cada vez más competitivo. Estados Unidos y Asia están aplicando políticas agresivas para atraer la innovación biomédica, lo que ha llevado a que Europa haya perdido un 25% de su cuota de I+D en las dos últimas décadas, en beneficio de estas regiones.
«Tenemos el potencial para ser líderes en la investigación, desarrollo y producción de nuevos medicamentos, pero los cambios geopolíticos están transformando el panorama mundial de innovación en salud y es necesario actuar con urgencia para no perder la carrera global por la innovación. Es fundamental aprovechar estas fortalezas y adoptar medidas políticas decididas para que Europa pueda seguir siendo competitiva en la carrera global por la inversión farmacéutica», subraya Juan Yermo, director general de la Farmaindustria.
Europa ha perdido en las dos últimas décadas un 25% de cuota de I+D, en detrimento de Estados Unidos y Asia
Agilizar ensayos y ampliar la investigación a atención primaria
Para mantener esta posición, el sector considera imprescindible que Europa consolide y amplíe la simplificación de los procesos de autorización de ensayos clínicos, en línea con iniciativas como Fast Eu y la futura Biotech Act. El objetivo es reforzar la competitividad europea, atraer inversiones y acelerar el acceso de los pacientes a tratamientos innovadores.
En este contexto, Farmaindustria ha intensificado en el último año proyectos para ampliar el alcance de la investigación clínica, entre ellos la extensión de los ensayos a los centros de salud. Este avance se ha materializado con la puesta en marcha de los Mapas y Observatorios Autonómicos de Investigación Clínica en Atención Primaria.
Asimismo, la asociación ha trabajado en el impulso de procedimientos de evaluación acelerada para ensayos de fase I, inicialmente centrados en terapias avanzadas y enfermedades raras y posteriormente ampliados a medicamentos biológicos oncológicos, con el objetivo de mantener a España en la vanguardia de la investigación clínica europea.