Redacción Farmacosalud.com

Fuente: Hospital de Bellvitge (HUB) / ADmit Therapeutics / IDIBELL
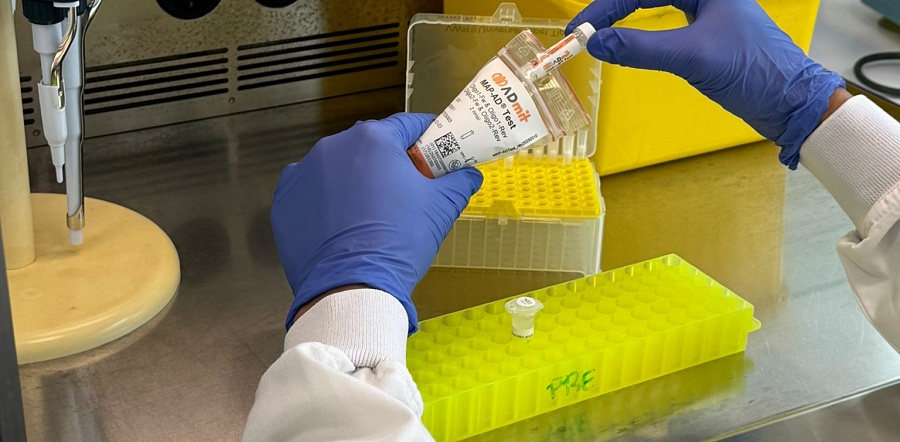
El Hospital de Bellvitge (l’Hospitalet de Llobregat, en Barcelona) ha tenido un papel clave en la validación clínica de un nuevo biomarcador en sangre que, por primera vez, permite anticipar la progresión del deterioro cognitivo leve hacia la demencia de Alzheimer. A diferencia de otros biomarcadores en sangre desarrollados por equipos internacionales, que sirven para confirmar la presencia de patología cerebral, el nuevo test MAP-AD® es pronóstico y aporta información clínica decisiva sobre la evolución futura de cada paciente.
Los resultados de la investigación, publicados en la revista ‘iScience’ (Cell Press), han permitido desarrollar el test MAP-AD, creado por la compañía ADmit Therapeutics, spin-off surgida del Instituto de Investigación Biomédica de Bellvitge (IDIBELL). Este test ha obtenido también el marcado CE-IVDR, que certifica que cumple los estrictos requisitos de seguridad y eficacia de la Unión Europea y abre la puerta a su aplicación clínica.
Biomarcadores mitocondriales
El ensayo observacional multicéntrico ha sido coordinado por el Dr. Jordi Gascón, jefe de la Unidad de Memoria del Servicio de Neurología del Hospital de Bellvitge, y ha contado con la participación del Dr. Ramón Reñé y el Dr. Jaume Campdelacreu, también neurólogos del centro. La investigación ha incluido muestras de pacientes con deterioro cognitivo leve y de personas voluntarias sin afectación cognitiva, procedentes de varios hospitales (Hospital Clínic de Barcelona, Hospital de la Santa Creu i Sant Pau, Consorci Sanitari Integral, Fundación CITA-Alzheimer) y de los biobancos de la Universidad de Washington y el Australian Imaging, Biomarker and Lifestyle Study.
MAP-AD es un análisis de sangre cualitativo que mide nuevos biomarcadores mitocondriales (metilación del ADN mitocondrial) y los combina con datos clínicos para predecir con alta precisión qué pacientes con deterioro cognitivo leve progresarán hacia la demencia de Alzheimer y cuáles se mantendrán estables.

Dr. Jordi Gascón
Fuente: Hospital de Bellvitge (HUB) / ADmit Therapeutics / IDIBELL
Según el Dr. Gascón, “durante años hemos podido identificar la patología subyacente, pero era muy difícil predecir la evolución clínica. Disponer de una herramienta fiable que anticipe la progresión es un punto de inflexión: nos permite mantener conversaciones más informadas con las familias y guiar mejor las intervenciones, ya sean preventivas, en ensayos clínicos o con las nuevas terapias emergentes”.
Por su parte, la Dra. Marta Barrachina, CEO y cofundadora de ADmit Therapeutics, destaca: “la certificación europea y la publicación científica en ‘iScience’ refuerzan la solidez de nuestro test. Es un paso fundamental porque, a diferencia de otros biomarcadores que sólo confirman patología, el MAP-AD anticipa la evolución clínica. Esto lo hace único y abre una nueva vía para mejorar la atención a las personas con riesgo de Alzheimer”.
Reducción de la lista de espera para la primera visita de 12 meses a sólo 15 días
El desarrollo de esta prueba coincide con la puesta en marcha de la nueva Unidad de Memoria del Hospital de Bellvitge, que ha transformado la atención a las personas con deterioro cognitivo. Este modelo integral y multidisciplinar ha reducido la lista de espera para la primera visita de 12 meses a únicamente 15 días.
En una sola mañana se integran las valoraciones médicas, neuropsicológicas, de enfermería y de trabajo social, mejorando la experiencia del enfermo y del cuidador. Además, la unidad impulsa medidas innovadoras como aplicaciones digitales, programas de apoyo a los cuidadores y nuevas líneas de investigación en demencias. “Es un proyecto que mejora la calidad de vida de pacientes y cuidadores y establece una base sólida para el trabajo en red”, afirma Gascón.

Fuente: Hospital de Bellvitge (HUB) / ADmit Therapeutics / IDIBELL
Referencia bibliográfica
Gascon-Bayarri, J. et al. Mitochondrial methylcytosines as blood-based biomarkers for Alzheimer’s disease dementia prognosis. iScience, 2025. DOI: 10.1016/j.isci.2025.113418