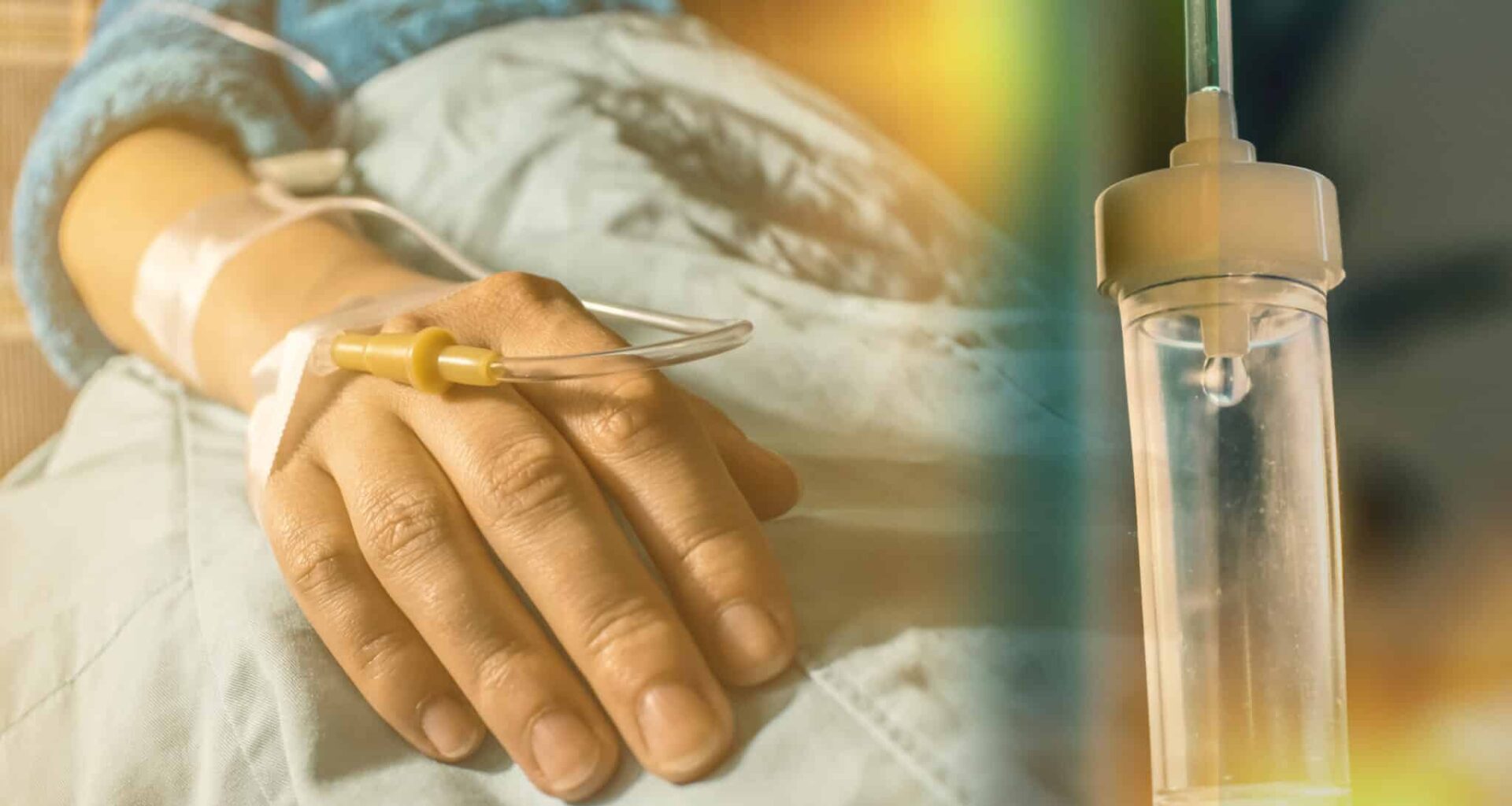
Le cancer est une bataille acharnée
entre les traitements agressifs et la survie des patients. Parmi
les armes les plus courantes, la chimiothérapie joue un rôle
essentiel en ciblant les cellules cancéreuses à division rapide.
Pourtant, un paradoxe persiste : ces médicaments, tout en
détruisant les tumeurs, peuvent aussi endommager les cellules
saines, en particulier celles qui se renouvellent rapidement, comme
les cellules sanguines. Une nouvelle étude publiée dans Nature
Genetics met en lumière ce double tranchant avec une
précision inédite, en identifiant comment certains traitements
accélèrent « artificiellement » le vieillissement des cellules
saines, et ce, de façon variable selon les médicaments
utilisés.
Comprendre l’impact de la
chimiothérapie sur les cellules saines
La chimiothérapie agit en
provoquant des cassures et des mutations dans l’ADN des cellules,
entraînant la mort des cellules tumorales. Or, certaines cellules
normales, notamment les cellules souches sanguines, partagent cette
caractéristique de division rapide. Leur ADN peut aussi être abîmé,
entraînant des mutations qui s’accumulent au fil du temps.
Pour évaluer précisément cet
effet, des chercheurs ont analysé le sang de 23 patients ayant reçu
divers traitements de chimiothérapie et l’ont comparé à celui de 9
individus sains. Leur approche innovante consistait à isoler et
séquencer l’ADN des cellules souches sanguines, pour détecter les «
signatures mutationnelles » — ces schémas particuliers de mutations
qui reflètent le type de dommages causés par différents
médicaments.
Quatre nouvelles signatures
mutationnelles liées à la chimiothérapie
L’étude a révélé l’existence
de quatre nouvelles signatures mutationnelles associées à la
chimiothérapie, jusque-là inconnues dans la base de données
mondiale COSMIC. Ces mutations sont présentes uniquement chez les
patients traités, et varient selon les médicaments administrés.
Par exemple, certains agents
alkylants et composés à base de platine, couramment utilisés, sont
responsables de plus de mutations, tandis que d’autres médicaments
comme le cyclophosphamide génèrent beaucoup moins d’altérations
génétiques, ce qui pourrait expliquer pourquoi le risque de cancer
secondaire est plus faible avec ce dernier.
Quand les cellules sanguines
paraissent plus âgées qu’elles ne le sont
L’accumulation de mutations
dans l’ADN est un processus naturel lié au vieillissement.
Cependant, chez les patients traités par chimiothérapie, ce
vieillissement génétique est artificiellement accéléré. Dans
l’étude, un enfant de 3 ans sous chimiothérapie présentait dix fois
plus de mutations dans ses cellules sanguines que des enfants sains
du même âge. En termes simples, ses cellules semblaient
génétiquement plus vieilles que celles d’une personne de 80 ans
n’ayant jamais reçu de traitement.
Cette « vieillesse »
artificielle ne signifie pas forcément que les cellules vont se
transformer en cancer, mais elles accumulent un risque accru de
tumeurs secondaires. Ce risque est un facteur crucial dans la
gestion à long terme des patients, notamment ceux qui survivent
plusieurs années après le traitement initial.
Crédit :
iStock
Crédits :kckate16/istockVers une chimiothérapie plus
sûre : l’espoir des traitements personnalisés
Ces découvertes ouvrent la
voie à une meilleure sélection des protocoles de chimiothérapie. En
comprenant quels médicaments causent moins de dommages génétiques,
les médecins pourraient choisir des traitements aussi efficaces
contre le cancer, mais moins nocifs pour les cellules saines.
Par exemple, dans certains
lymphomes hodgkiniens, des combinaisons alternatives de
chimiothérapie ont montré une efficacité équivalente tout en
réduisant les mutations secondaires. Cela est particulièrement
encourageant pour les cancers avec un bon taux de guérison, où la
prévention des effets secondaires à long terme est primordiale.
Cependant, dans des cancers
plus agressifs avec des taux de survie plus faibles, il faut
d’abord assurer la guérison avant d’optimiser la toxicité des
traitements. Comme le souligne un expert du Memorial Sloan
Kettering Cancer Center, il est indispensable de guérir le cancer
avant de réduire la toxicité.
Limites et perspectives
futures
L’étude présente certaines
limites, notamment la taille modeste de l’échantillon et le fait
que les analyses ont été faites sur des cellules sanguines en
éprouvette, ce qui ne reproduit pas parfaitement l’environnement
naturel du corps. Les chercheurs souhaitent étendre leurs travaux à
des cohortes plus larges et utiliser des échantillons de sang
circulant.
Malgré ces limites, ce travail
constitue une avancée majeure dans la compréhension des effets
collatéraux de la chimiothérapie, et pourrait bientôt contribuer à
une médecine plus personnalisée, alliant efficacité et protection
des cellules saines.